Penurunan Tekanan Uap Larutan Nonelektrolit
Menghitung Besar Penurunan Tekanan Uap Larutan Nonelektrolit.
Seperti yang sudah dibahas di atas bahwa semakin banyak partikel zat terlarut semakin kecil tekanan uap nya.
Jadi besarnya penurunan tekanan uap tergantung pada jumlah partikel zat terlarut.
Hal ini dipelajari dan diteliti oleh Francios M Raoult, besarnya jumlah partikel zat terlaurt disebutkan fraksi mol zat terlarut (Xt).
Dikatakan Raoult bahwa besar tekanan uap PELARUT tergantung FRAKSI MOL zat pelarut.

Dengan Keterangan :
P = Tekanan uap jenuh LARUTAN
Po = Tekanan uap pelarut murni
Xp = Fraksi mol pelarut
Perhatikan hukum Raoult di atas dengan seksama,
1. coba jelaskan dengan benar mengenai besar tekanan uap jika tidak partikel zat terlarut (Xt = 0) murni semua zat pelarut (Xp = 1) !
2. coba jelaskan dengan benar mengenai besar tekanan uap jika ada partikel zat terlarut (Xt) dan sebagian besar zat pelarut (Xp = 1 - Xt) !
penyelesaian menurut hukum Raoult,
1. P = Xp . Po
diketahui Xp = 1 maka P = Po .....
artinya tekanan uap semuanya adalah tekanan uap pelarut murni.
2. P = Xp . Po
diketahui Xp = 1 - Xt maka P = Po - Xt.Po....
artinya tekanan uap nya adalah tekanan uap pelarut murni dikurangi besar perkalian Xt.Po
dapat disimpulkan bahwa,
Jika tidak ada zat terlarut maka tekanan uap nya merupakan tekanan uap pelarut murni nya.
Jika ada zat terlarut maka tekanan uap nya adalah tekanan uap pelarut murni dikurangi perkalian Xt.Po
Penurunan tekanan dari Po ke P disebut Penurunan Tekanan Uap (ΔP) dirumuskan dengan,
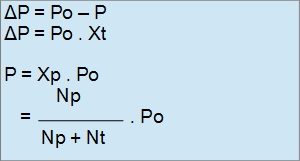
Dengan Keterangan :
ΔP : Penurunan Tekanan Uap
P : Tekanan Uap Jenuh Larutan
Po : Tekanan Uap Pelarut Murni
Xp : Fraksi Mol Pelarut
np : Mol Pelarut
nt : Mol Zat Terlarut
Perhatikan Rumus ΔP = Po - P dan ΔP = Po.Xt di atas dengan seksama,
coba jelaskan dengan benar mengenai perubahan rumus ΔP = Po - P menjadi ΔP = Po.Xt
Rumus Penurunan Tekanan Uap (ΔP) adalah
ΔP = Po - P
ΔP = Po - P ...karena P = Po - Xt.Po.....maka ΔP = Po - (Po - Xt.Po) = Po - Po + Xt.Po = Xt.Po atau ΔP = Po.Xt
Faraksi mol (X) dalam hal ini dinyatakan sebagai bentuk perbandingan antara mol suatu spesies dengan mol total dimana spesies itu berada.
fraksi mol zat terlarut (Xt) ......
rumusnya, Xt = nt / (np + nt)
fraksi mol zat pelarut (Xp) .......
rumusnya Xp = np / (np + nt)
Total seluruh fraksi mol tiap zat yang ada di dalam larutan tetap satu, satu larutan.
Xt + Xp = 1
Jadi jika dicontohkan suatu larutan dibuat dari pelarut air dan zat terlarut berupa urea. Maka fraksi mol pada masing – masing zat adalah sebagai berikut:
X air = mol air / mol air + mol urea dan
X urea = mol urea / mol air + mol urea
Jumlah fraksi mol untuk setiap penyusun campuran apabila dijumlahkan akan kita peroleh nilai = 1, untuk fraksi mol larutan urea diatas maka dapat dinyatakan :
X air + X urea = 1
Persamaan 3 inilah yang dapat kita pakai untuk mengetahui berapa besarnya penurunan uap suatu larutan. Untuk mencari penurunan tekanan uap kita bisa melihat melalui persamaan 1 atau pun 3. Yang perlu kita ingat adalah jika kita menggunakan rumus 1 maka fraksi mol yang dipakai adalah Xp (fraksi mol pelarut) namun jika menggunakan rumus 3 maka fraksi mol yang dipakai adalah Xt (fraksi mol zat terlarut). Itulah perbedaan mendasar dari kedua persamaan diatas. (Baca Juga : Perbedaan Larutan Elektrolit dan Non Elektrolit)
Bagaimana jika zat terlarut di dalam suatu pelarut bersifat volatile?
Penjelasan diatas lebih kita utamakan kepada suatu larutan yang sifat zat terlarutnya adalah nonvolatile, sedangkan untuk larutan yang dibangun dari zat terlarut yang bersifat volatile?
Contoh campuran ini adalah bensena – toluena, air – etanol, atau aseton – etil asetat. Karena dengan zat terlarut yang bersifat volatile maka uap zat terlarut ini akan bereaksi terhadap total uap larutan. Uap yang ada didalam larutan jenis ini didapatkan dari molekul zat terlarut dan molekul pelarut.
Setelah membaca penjelasan diatas maka total tekanan uap larutan dapat dinyatakan dengan rumus:

Perlu kita ingat bahwa Hukum Raoult hanya berlaku untuk larutan yang bersifat ideal atau larutan dengan konsentrasi rendah. Dimana larutan ideal dicapai jika interaksi antara solute – solut, solvent – solvent, solute – solvent diperoleh nilai yang hampir sama. Campuran yang memenuhi Hukum Raoult atau bersifat ideal contohnya adalah bensena – toluena. Pencampuran keduanya akan menghasilkan entalpi yang hampir bernilai nol “0” sehingga campuran ini bersifat “ideal”.
Apabila ketika pelarutan zat terlarut ke dalam suatu pelarut dibebaskan panas (eksoterm) maka entalpinya akan bernilai negative, kita dapat mengasumsikan bahwa terjadi suatu interaksi yang kuat antara zat pelarut dan zat terlarut, hal ini bisa menyebabkan pelarut memiliki tendensi yang lebih kecil untuk menguap dan nilai tekanan uap larutannya akan jauh lebih kecil dibandingkan dengan nilai yang ditentukan dari hukum Raoult itu sendiri, kejadian ini disebut sebagai “deviasi negative hukum Raoult”. Contohnya yaitu melarutkan zat aseton dengan air atau campuran antara kloroform dengan zat aseton. Interaksi kuat antara aseton – air atau aseto – klorofom diakibatkan oleh adanya ikatan hidrogen diantara keduanya.
Contoh Soal Penurunan Tekanan Uap Larutan
1. Tekanan uap air pada suhu 25 0C adalah 23,76 mmHg. Jika pada suhu yang sama, kedalam 900 mL air ditambahkan urea (Mr = 60 g/mol), tekanan uap larutan menjadi 22,84 mmHg. Penurunan tekanan uap larutan tersebut adalah…
Diketahui:
T = 25 0C
Po = 23,76 mmHg.
V = 900 mL
Mr = 60 g/mol.
P = 22,84 mmHg.
Ditanya: ΔP = …
Jawab:
Ditanya: ΔP = …
Jawab:
ΔP = P0 – P = 23,76 mmHg – 22,84 mmHg = 0,92 mmHg
2. Tekanan uap air pada suhu 25 0C adalah 23,76 mmHg. Jika pada suhu yang sama, kedalam 900 mL air ditambahkan urea (Mr = 60 g/mol), tekanan uap larutan menjadi 22,84 mmHg. Fraksi mol larutan tersebut adalah….
Pembahasan
Diketahui:
T = 25 0C
P0 = 23,76 mmHg.
V = 900 mL
Mr = 60 g/mol.
P = 22,84 mmHg.
Ditanya: xp = …
Jawab:
Ditanya: xp = …
Jawab:
xp = ΔP / P0 = 0,92 mmHg / 23,76 mmHg
xp = 0,0387
3. Fraksi mol urea dalam air adalah 0,5. Tekanan uap air pada 20°C adalah 17,5 mmHg. Berapakah tekanan uap jenuh larutan tersebut pada suhu tersebut?
Penyelesaian:
Penyelesaian:
Diketahui :
xA = 0,5
P0 = 17,5 mmHg
Ditanya : P …?
Jawab : ΔP = xA ⋅ P0
= 0,5 ⋅ 17,5 mmHg
= 8,75 mmHg
P = P0 – ΔP
= 17,5 mmHg – 8,75 mmHg
= 8,75 mmHg
P0 = 17,5 mmHg
Ditanya : P …?
Jawab : ΔP = xA ⋅ P0
= 0,5 ⋅ 17,5 mmHg
= 8,75 mmHg
P = P0 – ΔP
= 17,5 mmHg – 8,75 mmHg
= 8,75 mmHg
Jadi begitulah penjelasan tentang Penurunan tekanan uap. Contoh penurunan tekanan uap di kehidupan sehari hari adalah pada kolam renang apung ditempat wisata yang mengadopsi ciri khas dari laut mati yang apabila anda berenang anda tidak akan tenggelam. Hal ini dikarenakan di laut mati zat terlarut yang sangat tinggi. Semoga bermanfaat untuk anda.
Komentar
Posting Komentar